Aromáticos
| Aromático más importante: benceno |
 Estructuras de frontera mesoméricas de benceno con seis electrones π en dobles enlaces deslocalizados , uno de los compuestos aromáticos más simples. (Nota: las presentaciones de arriba y de abajo son equivalentes). |
 Los electrones deslocalizados y la igualdad de los enlaces de la molécula de benceno están simbolizados por un círculo. |
 Fórmula histórica de benceno de Kekulé de la publicación original. |
Los compuestos aromáticos , o aromáticos para abreviar , son una clase de sustancias en la química orgánica . Su nombre proviene del olor aromático de los compuestos de esta clase de sustancias que se descubrieron por primera vez.
Las moléculas aromáticas tienen al menos un sistema de anillos que, según la regla de Hückel , contiene un número de 4n + 2 (n = 0,1,2, ...) electrones deslocalizados en dobles enlaces conjugados , pares de electrones libres u orbitales p desocupados . Esta deslocalización conduce a un sistema de enlace especial en el que no es posible distinguir entre enlaces simples y dobles en el anillo. En sistemas de anillos simples y simétricos como el benceno , todos los enlaces son idénticos. En las fórmulas estructurales , todas las estructuras de los límites mesoméricos se muestran para mayor claridad o los enlaces simples se proporcionan con un anillo (a veces discontinuo), que simboliza los electrones deslocalizados. Los aromáticos se comparan con los alifáticos d. H. Los sistemas de doble enlace no aromáticos tienen menos energía y, por lo tanto, son menos reactivos . En particular, no son propensos a reacciones de adición .
Criterios de aromaticidad
Definiciones históricas
- El benceno es el compuesto aromático más simple con el que todos los demás aromáticos están relacionados por estructura. Suelen tener un olor aromático agradable. El nombre Aromat, de la palabra griega 'aroma' = 'fragancia', se deriva de este olor típico.
Sin embargo, los aromáticos no pueden definirse por el olor, ya que con una masa molar alta o sustituyentes fuertemente polares, a menudo no se percibe ningún olor.
- Los aromáticos son compuestos poliinsaturados que son relativamente inertes a la adición en el doble enlace y que, en cambio, entran en una sustitución con relativa facilidad directamente en un doble enlace .
Esta determinación del nombre, que permite una distinción experimental, fue válida en el siglo XX, por ejemplo, incluso antes de que se aclararan la estructura y las relaciones de unión. En la actualidad, se suele preferir una definición más general de estructura electrónica. Las propiedades especificadas - en resumen: sustitución en lugar de adición - son, por supuesto, características y características muy importantes.
- El sistema de enlace aromático muestra una estabilidad particular, que puede determinarse, por ejemplo, comparando la entalpía de hidrogenación del aromático con un correspondiente compuesto de referencia no aromático e hipotético (en el caso del benceno, ciclohexatrieno) como energía de resonancia .
- La frecuencia de resonancia de los átomos de hidrógeno en el experimento de resonancia magnética nuclear es característica. Esto se manifiesta en un fuerte cambio hacia abajo para los protones fuera del sistema aromático y un cambio hacia arriba para los protones dentro del sistema aromático.
Definición de aromáticos
Requisitos previos necesarios pero no suficientes para un aromático:
- Una molécula cíclica , es decir, tiene al menos un anillo, que en muchos casos es un anillo de benceno .
- Un sistema de doble enlace que está completamente conjugado a través del anillo .
Ellos son- varios dobles enlaces , cada uno de los cuales está separado exactamente por un
- uno o más dobles enlaces separados por átomos de carbono cargados positiva o negativamente o por heteroátomos .
Esta condición es sinónima y más breve:
- todos los átomos del anillo son sp 2 - hibridado .
Un aromático está presente si también se cumplen las siguientes condiciones:
- El sistema de doble enlace es plano; En casos excepcionales, se permiten ligeras desviaciones del nivel. Por ejemplo, en algunos ciclofanos, la unidad de benceno se deforma en forma de bote en un ángulo de hasta 30 °.
- El número de electrones deslocalizados debe cumplir con la regla de Hückel, es decir , en el sistema de electrones conjugados debe haber 2 o 6 o 10 o 14 ... electrones:
La regla de Hückel establecida por Erich Hückel está representada principalmente por la fórmula (4n + 2) π electrones (n = 0,1,2,3…), deslocalizados sobre todos los átomos del anillo del sistema. Los sistemas cíclicos π conjugados con 4n π electrones (n = 1,2,3…) se denominan antiaromáticos .
La estructura básica de muchos compuestos aromáticos es el benceno C 6 H 6 . (La regla de Hückel se cumple aquí con n = 1: el benceno tiene 6 electrones π). Por lo tanto, el benceno se considera uno de los hidrocarburos aromáticos más simples , especialmente desde que se descubrieron las propiedades especiales de los compuestos aromáticos en el benceno y sus derivados . El benceno es más estable que un ciclohexatrieno hipotético (es decir, no producible) con dobles enlaces localizados y, por lo tanto, menos reactivo.
Iones aromáticos

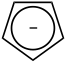
Dado que, de acuerdo con la regla de Hückel , un sistema conjugado cíclico plano con 2 electrones π también se considera aromático, las sales de ciclopropenilo también contienen cationes aromáticos:

El ion ciclopropenilio cumple la regla de Hückel con n = 0 y, por lo tanto, es uno de los compuestos aromáticos más pequeños posibles en términos tanto del número de electrones deslocalizados como del tamaño del anillo.
El anión ciclopentadienilo cargado negativamente , que se encuentra en metalocenos como el ferroceno, también es aromático :
Al igual que con el benceno, n = 1 aquí.
Reacciones aromáticas
Las más importantes son las reacciones de sustitución , por ejemplo
- Sustitución aromática electrofílica , como sulfonación , nitración , acilación de Friedel-Crafts , acoplamiento azo , cloración , bromación . Se aplican reglas especiales a la sustitución secundaria electrofílica en aromáticos . Los sustituyentes ya presentes en el aromático "dirigen" la sustitución adicional a ciertas posiciones .
- Sustitución aromática nucleofílica
- Desaromatización : Pérdida del sistema aromático por reducción adecuada.
Clasificación de aromáticos
Criterios
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
Hay una gran cantidad (se conocen varios millones) de diferentes compuestos aromáticos . Se pueden dividir en grupos según varios criterios:
- Dado que la aromaticidad solo está ligada a la deslocalización cíclica de electrones y, por lo tanto, no está restringida a compuestos orgánicos , el fenómeno de aromaticidad también se encuentra en compuestos puramente inorgánicos . Un aromático inorgánico es, por ejemplo, borazol B 3 N 3 H 6 , que puede derivarse formalmente de benceno C 6 H 6 reemplazando los átomos de carbono alternativamente con átomos de nitrógeno o átomos de boro . Sin embargo, la aromaticidad del borazol es mucho menos pronunciada que la de z. B. en el caso del benceno (discusión detallada bajo borazol). La densidad de electrones π está fuertemente localizada en los átomos de nitrógeno y no se distribuye uniformemente entre todos los átomos del anillo. Aunque el compuesto original todavía muestra una geometría plana, el anillo en los complejos de carbonilo metálico adopta una conformación ondulada en contraste con el benceno. La reactividad cuando el anillo es atacado por nucleófilos o electrófilos (en contraste con el benceno inerte) es un signo de una clara polarización del enlace.
- Los sistemas de anillos que solo constan de átomos de carbono se denominan carbociclos . Por tanto, el benceno C 6 H 6 y el naftaleno C 10 H 8 pertenecen a los carbociclos. Por el contrario, como todos los heterociclos en el sistema de anillo, los heteroaromáticos contienen otros átomos como nitrógeno, por ejemplo en la piridina aromática C 5 H 5 N. (La piridina se deriva formalmente del benceno reemplazando un grupo de átomos C - H con N.)
- Los aromáticos carbocíclicos (= con una estructura aromática de átomo de carbono) se pueden dividir en hidrocarburos (aromáticos) y aromáticos sustituidos (según la clasificación de compuestos orgánicos). El benceno C 6 H 6 y el tolueno C 6 H 5 -CH 3 son hidrocarburos, el fenol C 6 H 5 -OH y el trinitrotolueno TNT C 6 H 2 (NO 2 ) 3 (CH 3 ) son compuestos derivados de los mismos por sustitución.
- Otra clasificación se basa en el número de ciclos aromáticos : uno de los compuestos aromáticos más simples, el benceno, consta exactamente de un anillo. Naftaleno C 10 H 8 es una bicicleta , tiene un sistema π aromático con 10 electrones π, que se distribuye en los dos anillos.
- Los aromáticos con varios anillos se pueden dividir en aquellos en los que los anillos tienen átomos comunes ( anillos fusionados o fusionados ), como en el naftaleno C 10 H 8 , o aquellos con anillos separados (aislados), por ejemplo, bifenilo C 6 H 5 -C 6 H 5 .
- Se puede realizar una clasificación adicional según el número de átomos del anillo en el sistema aromático. Son típicos seis átomos de anillo, por ejemplo, en benceno C 6 H 6 . Para formar un anillo cerrado, son necesarios al menos tres átomos, por lo que hay aromáticos con tres, cuatro, cinco, siete o más átomos.
- Según la carga del sistema aromático, por ejemplo, el anión ciclopentadienilo está simplemente cargado negativamente.
Ejemplos de compuestos aromáticos
Hidrocarburos
Los hidrocarburos aromáticos también se denominan arenos. Algunos ejemplos son:
- Benceno C 6 H 6
- Tolueno (metilbenceno) C 6 H 5 -CH 3
- Xileno (dimetilbenceno) H 3 C-C 6 H 4 -CH 3
- Mesitileno (trimetilbenceno) C 6 H 3 (CH 3 ) 3
Los hidrocarburos con varios anillos se denominan hidrocarburos aromáticos policíclicos (HAP), por ejemplo:
- Naftaleno C 10 H 8 (2 anillos; dos anillos de seis miembros)
- Azuleno C 10 H 8 (2 anillos; cinco / siete anillos)
- Antraceno C 14 H 10 (3 anillos)
Los anulenos , es decir , los hidrocarburos cíclicos con dobles enlaces conjugados, pueden tener aromaticidad. Después del benceno, el [14] -anuleno es el anuleno aromático más pequeño, y los anulenos con 18 y 22 átomos de carbono también son aromáticos.
Iones aromáticos
| ||||||||
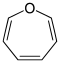
Los compuestos parentales típicos de esta clase son el ion ciclopropenilio con 2π electrones, el anión ciclopentadienilo, el catión cicloheptatrienilo y el ion pirilio con 6π electrones. En el caso del ion pirilio, el oxígeno aporta dos electrones al sistema π deslocalizado a través de uno de los dos pares de electrones libres. El segundo par solitario de electrones se encuentra en el plano del anillo y, por lo tanto, no contribuye al sistema π deslocalizado (análogo al par solitario de electrones en el nitrógeno de la piridina).
Derivados de benceno
- Fenol C 6 H 5 -OH
- Nitrobenceno C 6 H 5 -NO 2
- Anilina (aminobenceno) C 6 H 5 -NH 2
- Hidroquinona HO-C 6 H 4 -OH
- Ácido pícrico (2,4,6-trinitrofenol) C 6 H 2 (OH) (NO 2 ) 3
Heteroaromáticos
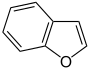
- Furano C 4 H 4 O (anillo de cinco miembros con átomo de oxígeno)
- Tiofeno C 4 H 4 S (anillo de cinco miembros con átomo de azufre)
- Piridina C 5 H 5 N (anillo de seis miembros con átomo de nitrógeno)
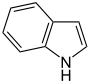
- Pirrol C 4 H 4 NH (anillo de cinco miembros con átomo de nitrógeno e hidrógeno)
Compuestos aromáticos halógenos
- Clorobenceno C 6 H 5 -Cl
- Bromofenoles Br-C 6 H 4 -OH
Anti-aromáticos
Ver artículo principal: Antiaromat
| |||||
Los antiaromáticos son sustancias que cumplen las tres primeras condiciones de un aromático (dobles enlaces cíclicos, planos, conjugados), pero tienen 4n electrones π en lugar de 4n + 2 π electrones . Según la aproximación de Hückel, los antiaromáticos experimentan poca o ninguna estabilización debido a la deslocalización cíclica. Debido a la regla de Hund , los orbitales moleculares degenerados en pares deben estar ocupados cada uno por un electrón. De acuerdo con la aproximación, los antiaromáticos están presentes como radicales triplete altamente reactivos. El antiaromático más simple, el ciclobutadieno , solo es estable a temperaturas muy bajas (≤ 20 K ) en una matriz sólida. El tri- terc- butilciclopentadieno, por otro lado, es estable durante algunas horas a 20 ° C. Curiosamente, el ciclobutadieno es estable como ligando en la química organometálica , un ejemplo es el complejo ciclobutadieno-hierro tricarbonilo.
El ciclooctatetraeno tiene 8 electrones π. Sin embargo, no es plano, por lo que los dobles enlaces no se conjugan. Por tanto, la regla de Hückel no se puede aplicar. El 1,3,5,7-ciclooctatetraeno es, por tanto, no aromático.
Los antiaromáticos son un subconjunto de los compuestos alicíclicos no aromáticos . Estos últimos también incluyen compuestos no conjugados.
Aromáticos de moebius
El 1964 de Edgar Heilbronn predijo que la Aromaticidad de Möbius implica que los orbitales π ocupados en un sistema cíclico p-conjugado como una banda de Mobius están dispuestos, es decir, con una rotación de 180 °. Además, los orbitales π están ocupados por 4n electrones (donde n es un número natural aquí ). Los aromáticos de Möbius son quirales debido al giro . Heilbronner ahora llegó a la conclusión de que los sistemas de Möbius nunca pueden ser más bajos en energía que sus homólogos de Hückel. El problema con él era que asumía una rotación solo para el cálculo de las moléculas de Möbius, pero no para las de Hückelschen. Un año después, Zimmerman había examinado más de cerca el problema.
Sigue siendo motivo de controversia si una molécula sintetizada por Rainer Herges en 2003 realmente representa un aromático de Möbius o solo tiene la topología necesaria .
Aromáticos en la naturaleza

Muchos compuestos de la naturaleza tienen estructuras aromáticas. Son omnipresentes en las proteínas , los aminoácidos como la tirosina , el triptófano o la fenilalanina . El ADN o ARN , los portadores de información genética , contienen la nucleobase adenina como parte del nucleótido ATP . Los tintes vegetales como los flavonoides solubles en agua , la lignina constructora de la madera , los cofactores de enzimas como el fosfato de piridoxal o las pterinas son solo algunos ejemplos más.
En las hormonas sexuales femeninas naturales estradiol , estriol y estrona , el anillo A de la estructura de esteroides es aromático. Por el contrario, el anillo A en las hormonas sexuales masculinas ( andrógenos ) no es aromático.
La síntesis bioquímica y la descomposición de aromáticos a menudo se realizan mediante enzimas especiales . Al descomponer los aromáticos , los microorganismos también devuelven los aromáticos de la naturaleza inanimada, como contaminantes , pesticidas o desechos de la industria química, al ciclo del carbono .
Ver también
literatura
- Günther Maier: Aromático, ¿qué significa eso realmente? La química en nuestro tiempo , noveno año 1975, núm. 5, págs. 131-141, doi: 10.1002 / ciuz.19750090502 .
- Paul von Ragué Schleyer, Haijun Jiao: ¿Qué es la aromaticidad? En: Química pura y aplicada . cinta 68 , no. 2 , 1996, pág. 209-218 , doi : 10.1351 / pac199668020209 .
enlaces web
- Regla de Hückel (PDF; 27 kB) ( Memento del 13 de agosto de 2007 en Internet Archive )
Evidencia individual
- ↑ August Kekulé: Acerca de algunos productos de condensación del aldehído , Liebigs Ann. Chem. 1872 , 162 (1), págs. 77-124; doi: 10.1002 / jlac.18721620110 .
- ^ FA Carey, RJ Sundberg: Organische Chemie , VCH, Weinheim, 1995, ISBN 978-3-527-29217-2 .
- ↑ Joachim Buddrus: Fundamentos de la química orgánica , cuarta edición, de Gruyter Verlag, Berlín, 2011, p. 426, ISBN 978-3-11-024894-4 .
- ↑ E. Heilbronner: Orbitales moleculares Huckel de conformaciones de anulenos de tipo Mobius . En: Letras de tetraedro . cinta 5 , no. 29 , 1 de enero de 1964, pág. 1923-1928 , doi : 10.1016 / S0040-4039 (01) 89474-0 .
- ^ Howard E. Zimmerman: sobre diagramas de correlación orbital molecular, la aparición de sistemas de Möbius en reacciones de ciclación y factores que controlan las reacciones de estado de tierra y excitado. Yo . En: Revista de la Sociedad Química Estadounidense . cinta 88 , no. 7 , 1 de abril de 1966, págs. 1564-1565 , doi : 10.1021 / ja00959a052 .
- ^ Howard E. Zimmerman: diagramas de correlación orbital molecular, sistemas Mobius y factores que controlan las reacciones de tierra y estado excitado. II . En: Revista de la Sociedad Química Estadounidense . cinta 88 , no. 7 , 1 de abril de 1966, págs. 1566-1567 , doi : 10.1021 / ja00959a053 .
- ↑ D. Ajami, O. Oeckler, A. Simon, R. Herges: Síntesis de un hidrocarburo aromático de Möbius . En: Naturaleza . cinta 426 , no. 6968 , 2003, pág. 819–821 , doi : 10.1038 / nature02224 .
- ↑ Claire Castro, Zhongfang Chen, Chaitanya S. Wannere, Haijun Jiao, William L. Karney, Michael Mauksch, Ralph Puchta, Nico JR van Eikea Hommes, Paul von Ragué Schleyer Investigación de un supuesto hidrocarburo aromático de Möbius. El efecto de la benzannelación sobre la aromaticidad del anuleno de Möbius [4n] . En: J. Am. Chem. Soc. , 2005, 127 , págs. 2425-2432; doi: 10.1021 / ja0458165 .
- ↑ Carsten Schmuck , Bernd Engels, Tanja Schirmeister , Reinhold Fink: Química de los medicamentos , Estudios de Pearson, p. 493, ISBN 978-3-8273-7286-4 .