Espectro de emisión


Un espectro de emisión es el espectro electromagnético que emiten átomos , moléculas o materiales sin que se emita radiación electromagnética de la misma frecuencia. La contraparte de un espectro de emisión es el espectro de absorción . Mientras que los niveles de energía discretos producen un espectro de líneas , las bandas de energía producen un espectro continuo.
Espectro atómico
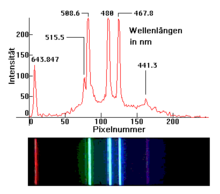
Un espectro atómico , el espectro de emisión de un solo átomo aislado , por lo que la intensidad de la luz emitida por ella ( emitida ) luz en función de la longitud de onda (o frecuencia). Las líneas espectrales individuales del espectro corresponden a la diferencia de energía entre dos estados diferentes del átomo, que puede ser aplicada, por ejemplo, por una partícula de luz absorbida ( fotón ) y luego emitida nuevamente en forma de otro fotón con esa energía. Esta diferencia de energía (o la línea en el espectro) es discreta , por lo que no puede asumir ningún valor, por lo que cada átomo, de acuerdo con su configuración electrónica específica , solo puede emitir fotones de longitudes de onda discretas muy específicas, que son características de los elementos químicos individuales .
El hecho de que las "líneas" en el espectro ("picos") sean precisamente curvas con un cierto ancho se basa en efectos cuánticos. Una comparación de las dos imágenes anteriores (1, 2) muestra que las "líneas" espectrales se ensanchan con el aumento de la presión del gas y el ancho de estas "líneas" puede aumentar tanto a una presión muy alta que prácticamente se crea un continuo de luz similar al de uno radiante. Sólido observado. La causa de este efecto es la frecuencia creciente de perturbaciones mutuas de los átomos cuando chocan con una presión creciente. El ejemplo de la línea espectral a 491,6 nm muestra claramente cuán fuertemente depende la intensidad relativa de esta línea de la presión de gas respectiva.
En la imagen inferior (3) se puede ver otra característica de las líneas espectrales del elemento cadmio.
Si un electrón se desprende completamente de su átomo por absorción de un fotón , esto se denomina ionización de este átomo, para lo cual, dependiendo del estado inicial del electrón, es necesaria una cierta energía mínima. Los suministros de energía por encima de esta energía mínima siempre conducen a la ionización, lo que explica por qué, a diferencia de lo dicho hasta ahora, los continuos son posibles en este rango de energía . El proceso inverso, es decir H. La emisión de un fotón cuando un electrón es capturado por un ion positivo se denomina recombinación , que, como acabamos de explicar, también puede producir una radiación continua, la denominada. Continuo de límites .
Espectro molecular
Como resultado de un espectro, un espectro molecular es el mismo que el espectro atómico descrito. Sin embargo, los niveles de energía son en su mayoría diferentes, por lo que las líneas relevantes están en el infrarrojo.
Espectro de emisión de un material sólido o líquido
Mientras que el espectro de emisión de gases diluidos da como resultado un espectro lineal , los sólidos y líquidos calientes emiten un espectro continuo porque los átomos individuales también interactúan entre sí y por lo tanto los estados cuánticos discretos se fusionan. Dicho espectro continuo se puede calcular multiplicando el espectro de un cuerpo negro ( ley de radiación de Planck ) de la misma temperatura por el coeficiente de absorción de la radiación electromagnética del "objeto" en la longitud de onda respectiva.
enlaces web
- Espectro de emisión y absorción a nivel escolar ( LEIFI )
- Video: espectro de absorción y emisión de sodio . Institute for Scientific Film (IWF) 2004, disponible en la Technical Information Library (TIB), doi : 10.3203 / IWF / C-14885 .
