5-fluorouracilo
| Fórmula estructural | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
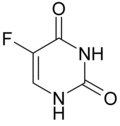
| |||||||||||||||||||
| Fórmula estructural del dioxo tautómero | |||||||||||||||||||
| General | |||||||||||||||||||
| Nombre no propietario | 5-fluorouracilo | ||||||||||||||||||
| otros nombres |
|
||||||||||||||||||
| Fórmula molecular | C 4 H 3 FN 2 O 2 | ||||||||||||||||||
| Breve descripción |
Polvo blanco |
||||||||||||||||||
| Identificadores / bases de datos externos | |||||||||||||||||||
| |||||||||||||||||||
| Información sobre medicamentos | |||||||||||||||||||
| Código ATC | |||||||||||||||||||
| Clase de droga | |||||||||||||||||||
| propiedades | |||||||||||||||||||
| Masa molar | 130,08 g · mol -1 | ||||||||||||||||||
| Estado fisico |
firmemente |
||||||||||||||||||
| Punto de fusion |
282–286 ° C (descomposición) |
||||||||||||||||||
| solubilidad |
soluble en agua (11,1 g l −1 a 22 ° C) |
||||||||||||||||||
| las instrucciones de seguridad | |||||||||||||||||||
| |||||||||||||||||||
| Datos toxicologicos | |||||||||||||||||||
| En la medida de lo posible y habitual, se utilizan unidades SI . A menos que se indique lo contrario, los datos proporcionados se aplican a condiciones estándar . | |||||||||||||||||||
El 5-fluorouracilo ( 5-FU ), también fluorouracilo ( DCI ), es un compuesto orgánico heterocíclico con una cadena principal de pirimidina y dos grupos carbonilo en las posiciones 2 y 4 y un flúor en la posición 5. Es un derivado de la nucleobase uracilo .
Es un fármaco que se utiliza como citostático en quimioterapia , especialmente en cáncer colorrectal y cáncer de mama . Fue desarrollado por el químico estadounidense Charles Heidelberger y comercializado en 1962 por la compañía farmacéutica Hoffmann-La Roche . Decisivas para la síntesis de 5-FU fueron las consideraciones de Heidelberger sobre el potencial inhibidor de tumores del fluoroacetato , la sal del ácido fluoroacético . Heidelberger describió más tarde el metabolismo del 5-FU con referencia al principio de síntesis letal ( biotransformación de fluoroacetato en fluorocitrato) desarrollado por el bioquímico británico e investigador de agentes de guerra Sir Rudolph Peters .
En pequeñas dosis y en combinación con ingredientes activos con ácido salicílico , 5-fluorouracilo también se utiliza para la aplicación externa como una verruga agente terapéutico bajo nombres comerciales tales como Verrumal ® .
propiedades
El 5-fluorouracilo es un sólido que se funde a 282-286 ° C con descomposición.
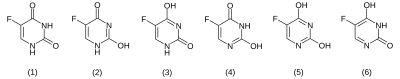
Hay seis posibles formas tautoméricas de 5-fluorouracilo en estado sólido, prefiriéndose la forma dioxo (1).
PROPIEDADES FARMACOLÓGICAS
efecto
El 5-fluorouracilo es un antimetabolito que durante la división celular debido a la similitud estructural con las bases pirimidínicas citosina y timina ( ADN - nucleótidos ) o uracilo ( ARN en lugar de nucleótido) de estas se incorpora en el ADN y ARN . La enzima pirofosforilasa UMP ( EC 2.4.2.9 ) convierte el 5-fluorouracilo en 5-fluoro-UMP, que luego se fosforila más a 5-fluoro-UTP y se incorpora al ARN . Esto provoca la síntesis de ARN defectuoso, que inhibe la biosíntesis de proteínas.
Además, el 5-flúor-dUMP también inhibe la timidilato sintasa ( EC 2.1.1.45 ), lo que finalmente conduce a la inhibición de la síntesis de ADN y la división celular.
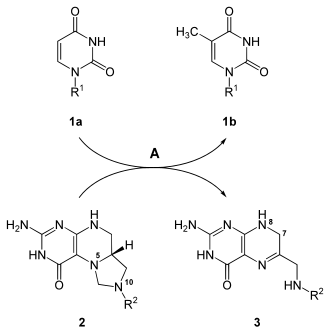 La síntesis de dTMP ( 1b ) a partir de dUMP ( 1a ) está catalizada por la timidilato sintasa ( A ), durante el cual N 5 , N 10 metileno tetrahidrofolato ( 2 ) se convierte en 7,8-dihidrofolato ( 3 ). El 5-flúor-dUMP inhibe la enzima y, por tanto, esta reacción.
La síntesis de dTMP ( 1b ) a partir de dUMP ( 1a ) está catalizada por la timidilato sintasa ( A ), durante el cual N 5 , N 10 metileno tetrahidrofolato ( 2 ) se convierte en 7,8-dihidrofolato ( 3 ). El 5-flúor-dUMP inhibe la enzima y, por tanto, esta reacción.
Es particularmente eficaz en la interfase del ciclo celular. Además de inhibir la síntesis de ADN y ARN, también inhibe el llamado complejo exosoma, esencial para la vida de la célula.
El 5-fluorouracilo se administra en forma de profármacos capecitabina o 5-fluorocitosina y solo se convierte en el metabolito activo en la célula. Por ejemplo, la 5-fluorocitosina es absorbida en la célula por una citosina permeasa e inmediatamente es desaminada allí por la citosina desaminasa para formar 5-fluorouracilo .
El efecto depende de la genética
Según un estudio, la eficacia depende de la genética del paciente. El polimorfismo de un solo nucleótido rs2612091 determina entonces la supervivencia esencial del cáncer gástrico localmente avanzado. La variante A / A se asocia con una buena efectividad, las variantes A / G y G / G se asocian con una efectividad significativamente menor. Es concebible que esto también se pueda transferir a otros cánceres. Pruebas genéticas , p . Ej. B. en forma de genotipado actualmente no es estándar en el tratamiento.
Efectos secundarios
Los efectos secundarios (náuseas, vómitos, inflamación de las mucosas, daño de la médula ósea) pueden ser considerables (ver el apartado de efectos secundarios en el artículo citostático ).
En experimentos con animales y estudios de pacientes, el daño cerebral causado por el daño a las células gliales se identificó como efectos secundarios a largo plazo . Los efectos secundarios neurotóxicos y cardiotóxicos se atribuyen al metabolito 5-FU, fluoroacetato.
Al agregar ácido tetrahidrofólico o ácido folínico , es posible una dosis más alta de 5-FU; este efecto se usa para terapias combinadas. El interferón-α también aumenta el efecto .
La degradación del 5-fluorouracilo tiene lugar a través de la enzima dihidropirimidina deshidrogenasa . En pacientes que se ven afectados por el trastorno metabólico hereditario poco común deficiencia de dihidropirimidina deshidrogenasa (DPD), el tratamiento con 5-fluorouracilo puede provocar una intoxicación extremadamente grave. Las personas afectadas suelen ser asintomáticas. El diagnóstico de exclusión se basa en el análisis de las purinas y pirimidinas y en la prueba específica "Exclusión de DPD en caso de tratamiento planificado con 5-fluorouracilo" de la orina.
El Comité de Evaluación de Riesgos de Farmacovigilancia (PRAC) de la Agencia Europea de Medicamentos (EMA) recomienda que los pacientes se sometan a pruebas de ausencia o deficiencia parcial de DPD antes de iniciar el tratamiento del cáncer con medicamentos que contienen fluorouracilo administrado mediante inyección o infusión (goteo). Esta recomendación se aplica en consecuencia al tratamiento con los principios activos relacionados capecitabina y tegafur , que se convierten en fluorouracilo en el organismo ( profármaco ).
Ver también
- Régimen de terapia FOLFOX
- Régimen de terapia FOLFIRI
Nombres comerciales
Benda-5 FU (D), Efudix (D, CH), Haemato-fu (D), Neofluor (D), Onkofluor (D), Ribofluor (D), varios genéricos (D, A, CH)
Verrumal (D, A, CH)
Evidencia individual
- ↑ a b c hoja de datos 5-fluorouracilo de Sigma-Aldrich , consultada el 2 de diciembre de 2013 ( PDF ).
- ↑ a b c Entrada sobre fluorouracilo en la base de datos ChemIDplus de la Biblioteca Nacional de Medicina de los Estados Unidos (NLM)
- ↑ a b Entrada sobre 5-fluorouracilo en la base de datos de sustancias GESTIS de la IFA , consultada el 23 de julio de 2016. (Se requiere JavaScript)
- ^ Charles Heidelberger: Pirimidinas fluoradas y sus nucleósidos . En: Agentes antineoplásicos e inmunosupresores (= Handbuch der experimental Pharmakologie / Handbook of Experimental Pharmacology ). Springer, Berlín, Heidelberg, 1975, ISBN 978-3-642-65808-2 , págs. 193-231 , doi : 10.1007 / 978-3-642-65806-8_12 .
- ↑ Katherine Elliott, Joan Birch (Ed.): Compuestos de carbono-flúor. Actividades Químicas, Bioquímicas y Biológicas. Associated Scientific Publishers, Amsterdam 1972, ISBN 978-0-470-71985-5 , págs. 130 .
- ↑ Joachim Morschhäuser: Resistencias y mecanismos de resistencia : ¿Cómo escapan los hongos de la terapia? en: Pharmazie en nuestro Zeit , 2003 , 32 (2), págs. 124-129 ( doi: 10.1002 / pauz.200390029 ).
- ^ F. von Bruchhausen: Hager's Handbook of Pharmaceutical Practice: Drugs AK , 5th edition, Springer Verlag, Berlín 1998, ISBN 3-540-61618-7 , p. 226.
- ↑ D. Meulendijks, EA Rozeman, A. Cats, K. Sikorska, M. Joerger: Variantes farmacogenéticas asociadas con el resultado en pacientes con cáncer gástrico avanzado tratados con fluoropirimidina y combinaciones de tripletes basados en platino: un análisis conjunto de tres estudios prospectivos . En: The Pharmacogenomics Journal . cinta 17 , no. 5 , octubre de 2017, pág. 441–451 , doi : 10.1038 / tpj.2016.81 .
- ↑ Ruolan Han, Yin M Yang, Joerg Dietrich, Anne Luebke, Margot Mayer-Pröschel, Mark Noble: El tratamiento sistémico con 5-fluorouracilo causa un síndrome de destrucción retardada de la mielina en el sistema nervioso central. En: Journal of Biology. 7, 2008, pág.12 , doi : 10.1186 / jbiol69 .
- ↑ Harold Koenig: Bases bioquímicas de la neurotoxicidad del fluorouracilo . En: Archives of Neurology . cinta 23 , no. 2 , 1 de agosto de 1970, pág. 155 , doi : 10.1001 / archneur.1970.00480260061008 ( jamanetwork.com [consultado el 30 de abril de 2018]).
- ^ H. Koenig, A. Patel: El síndrome cerebeloso agudo en la quimioterapia con 5-fluorouracilo: una manifestación de intoxicación por fluoroacetato . En: Neurología . cinta 20 , no. 4 , abril de 1970, pág. 416 , PMID 5535078 .
- ↑ Kazumasa Yamashita, Hideaki Yada, Toshihiko Ariyoshi: Efectos neurotóxicos de la alfa-fluoro-beta-alanina (FBAL) y el ácido fluoroacético (FA) en perros . En: Revista de Ciencias Toxicológicas . cinta 29 , no. 2 , mayo de 2004, pág. 155-166 , PMID 15206584 .
- ↑ M. Arellano, M. Malet-Martino, R. Martino, T. Spector: 5-Etiniluracilo (GW776): efectos sobre la formación de catabolitos tóxicos de 5-fluorouracilo, fluoroacetato y ácido fluorohidroxipropiónico en el modelo de hígado de rata perfundido aislado . En: British Journal of Cancer . cinta 76 , no. 9 , 1997, págs. 1170-1180 , PMID 9365165 , PMC 2228116 (texto completo gratuito).
- ↑ M. Arellano, M. Malet-Martino, R. Martino, P. Gires: El fármaco anticanceroso 5-fluorouracilo es metabolizado por el hígado de rata perfundido aislado y en ratas en fluoroacetato altamente tóxico. En: British Journal of Cancer . cinta 77 , no. 1 , 1998, pág. 79-86 , PMID 9459149 , PMC 2151255 (texto completo gratuito).
- ↑ S. Maurer, J. Thödtmann: El carcinoma de mama: diagnóstico y terapia. Govi-Verlag, Eschborn 2003, ISBN 978-3-7741-0996-4 .
- ↑ Van Kuilenburg ABP (2004) Dihidropirimidina deshidrogenasa y la eficacia y toxicidad del 5-fluorouracilo. Eur J Cancer 40: 939-950.
- ↑ Fluorouracil, Capecitabine, Tegafur and Flucytosine: Recomendación para pruebas y tratamiento , procedimiento de evaluación de riesgos del BfArM, notificación del 16 de marzo de 2020, consultado el 18 de marzo de 2020