Clorofilas

La clorofila (del griego antiguo χλωρός Chloros "verde claro, fresco" y φύλλον phyllon "hoja") o verde hoja se refiere a una clase de tintes naturales , que están formados por organismos que operan la fotosíntesis . Las plantas en particular obtienen su color verde de la clorofila.
Las plantas, las algas y las cianobacterias tienen diferentes tipos de clorofila, las bacterias que impulsan la fotosíntesis tienen diferentes tipos de bacterioclorofila .
Estructura y propiedades
Las clorofilas son estructuras moleculares llamadas complejos de quelatos , que consisten en un anillo de porfirina derivatizado y Mg 2+ como ion central. A diferencia de la porfirina, la estructura básica de las clorofilas contiene un quinto anillo adicional en el anillo III (numeración según Fischer). Dependiendo del tipo de clorofila, se unen diferentes cadenas laterales al cuerpo base. Por ejemplo, la clorofila a se esterifica con fitol (ver tabla). Las clorofilidas son clorofilas sin cadenas laterales.
Estructuralmente, las clorofilas están relacionadas con el hemo , que se presenta como un componente del pigmento sanguíneo ( hemoglobina ), la mioglobina y los citocromos , pero como ion central no contienen magnesio sino hierro . Las clorofilas son fácilmente solubles en etanol y acetona, así como en disolventes similares. Si la fotosíntesis tiene lugar en organismos que liberan oxígeno ( fotótrofos oxigenados ), generalmente se habla de clorofila . Sin embargo, los fotótrofos anoxigénicos no producen oxígeno como producto de reacción durante la fotosíntesis, en estos organismos la clorofila se llama bacterioclorofila .
Hans Fischer determinó la estructura molecular de la clorofila en 1940, la configuración absoluta fue aclarada por Ian Fleming en 1967 .
Estructura química de los fotótrofos oxigenados.
| Apellido | estructura | C 2 resto | C 3 resto | C 7 resto | C 8 resto | C 17 resto | C 17-18 enlace | Fórmula molecular |
|---|---|---|---|---|---|---|---|---|
| Clorofila a |

|
-CH 3 | -CH = CH 2 | -CH 3 | -CH 2 CH 3 | -CH 2 CH 2 COO- fitilo | Enlace sencillo | C 55 H 72 O 5 N 4 Mg |
| Clorofila b | -CH 3 | -CH = CH 2 | –CHO | -CH 2 CH 3 | -CH 2 CH 2 COO-Fitilo | Enlace sencillo | C 55 H 70 O 6 N 4 Mg | |
| Clorofila c 1 | -CH 3 | -CH = CH 2 | -CH 3 | -CH 2 CH 3 | -CH = CHCOOH | Doble enlace | C 35 H 30 O 5 N 4 Mg | |
| Clorofila c 2 | -CH 3 | -CH = CH 2 | -CH 3 | -CH = CH 2 | -CH = CHCOOH | Doble enlace | C 35 H 28 O 5 N 4 Mg | |
| Clorofila d | -CH 3 | –CHO | -CH 3 | -CH 2 CH 3 | -CH 2 CH 2 COO-Fitilo | Enlace sencillo | C 54 H 70 O 6 N 4 Mg | |
| Clorofila f | –CHO | -CH = CH 2 | -CH 3 | -CH 2 CH 3 | -CH 2 CH 2 COO-Fitilo | Enlace sencillo | C 55 H 70 O 6 N 4 Mg |
Estructura química de los fotótrofos anoxigénicos: bacterioclorofilas (Bchl)
un : No doble enlace entre C7 y C8 (marcado en el color en la imagen)
b : Bchl c , d y e son una mezcla de isómeros en los que el radical R 3 o R 4 es diferente sustituidos.
Propiedades espectrales
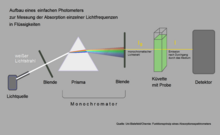
Se puede usar un espectrómetro de absorción simple para medir qué luz es absorbida de manera particularmente fuerte por la clorofila. En este ejemplo, la apertura se coloca de tal manera que la luz amarilla entra en la cubeta con la solución de clorofila. La cantidad de luz amarilla que emerge del otro lado de la cubeta apenas cae por debajo de la cantidad de luz incidente, porque la clorofila casi no absorbe nada en el rango de estas longitudes de onda. Si mueve el diafragma para que penetre la luz roja o azul, el detector detrás de la cubeta mide emisiones significativamente más bajas.
El espectro de absorción de en disolventes clorofilas disueltos siempre poseen dos máximos de absorción distinto de entre 600 y 800 nm, como la Q y - banda se hace referencia a, y uno en 400 nm, la banda de Soret se llama. La figura de la derecha muestra estos máximos de absorción para la clorofila a y b . Además, existe la banda Q x alrededor de 580 nm, que está polarizada perpendicularmente a Q y y generalmente absorbe muy débilmente. Para la clorofila a todavía se puede ver en la figura, para la clorofila b desaparece bajo tierra. El área entre las bandas se llama espacio verde .
Los espectros de la figura que sea fácil de entender por qué las hojas - que contienen clorofila una y b - son de color verde. En conjunto, la clorofila una y b absorben principalmente en el rango espectral azul (400-500 nm) y en la zona espectral roja (600-700 nm). En la zona verde, en cambio, no hay absorción, por lo que la luz verde se dispersa, lo que hace que las hojas parezcan verdes.

La absorción depende del disolvente y, en consecuencia, la posición de los máximos de absorción puede variar en unos pocos nanómetros según el tipo de disolvente. En el entorno natural de las clorofilas, es decir, el entorno de las proteínas, las cosas son diferentes. Aquí la posición de los máximos de absorción depende de dos factores: (1) Dependiendo de la carga parcial de los aminoácidos circundantes y la flexión de los grupos laterales de las moléculas de clorofila, los máximos de absorción pueden estar en longitudes de onda muy diferentes. (2) En las proteínas, las clorofilas se acercan mucho entre sí, de modo que interactúan entre sí ( interacción dipolo-dipolo ; a distancias muy cortas también intercambian interacción ). Esta interacción conduce a una disminución del nivel de energía y, por lo tanto, a un desplazamiento al rojo de los máximos de absorción. Esto se puede ver de manera particularmente impresionante en el ejemplo del complejo de antenas LH2 de bacterias púrpuras. El complejo LH2 consta de dos grupos de moléculas de bacterioclorofila dispuestas en un anillo (consulte la figura de la izquierda). El anillo superior (B850) contiene 18 moléculas BChl a , que están muy poco espaciadas entre sí, es decir , están fuertemente acopladas. El anillo inferior (B800) consta de 9 moléculas BChl a , que están significativamente más separadas y, por lo tanto, están mucho más débilmente acopladas.
El fuerte acoplamiento cambia la absorción de BChl a en el anillo B850 a rojo. La banda de absorción está a 850 nm. El BChl a débilmente acoplado del anillo B800, por otro lado, absorbe a 800 nm, es decir, aproximadamente en el mismo rango que las moléculas de BChl a disueltas en disolvente . En el espectro de absorción (figura de la derecha) del complejo LH2, las bandas de absorción de las moléculas B800 y B850-BChl- a están claramente separadas. Además, se muestran bandas que se originan a partir de moléculas de carotenoides , estas no se muestran en la estructura.
Tipos
Hay varios tipos de clorofila que se diferencian en los grupos laterales de la porfirina. Tienen diferentes espectros de absorción y ocurren en diferentes organismos fototróficos:
| Tipo de clorofila | color | Máximos de absorción (en nm) |
Ocurrencia |
|---|---|---|---|
| Clorofila a | azul verde | 430, 662 (en acetona) | Cianobacterias y todos los eucariotas fototróficos |
| Clorofila b | amarillo verde | 454, 643 (en éter dietílico) | Algas verdes ( Chlorophyta ), Euglenozoa y todas las plantas terrestres |
| Clorofila c | verde | 444, 576, 626 | en lugar de clorofila b en algas pardas ( Phaeophyta ), diatomeas ( Bacillariophyta ), algas doradas ( Chrysophyta ), algas verde amarillentas ( Xanthophyta ), Haptophyta , Dinophyta y Raphidophyceae |
| Clorofila d | 447, 688 | en lugar de clorofila b en algas rojas ( Rhodophyta ) | |
| Bacterioclorofila a | verde | 358, 577, 773 (en acetona) | Bacterias moradas ( Rhodospirillaceae , Chromatiaceae ) |
| Bacterioclorofila b | 368, 580, 794 (en acetona) | Bacterias de azufre púrpura ( Chromatiaceae ); Bacterias moradas | |
| Bacterioclorofila c | verde | 432, 660 (¿en acetona?) | Bacterias de azufre verde ( Chlorobiaceae ) |
| Bacterioclorofila c p | 740 ( in vivo ) | Bacterias verdes sin azufre ( Chloroflexaceae ) | |
| Bacterioclorofila d | 458, 646 (¿en qué?) 427, 654 (en acetona) | Bacterias de azufre verde ( Chlorobiaceae ) | |
| Bacterioclorofila e | 424, 654 (¿en qué?) 462, 649 (en acetona) | Bacterias de azufre verde ( Chlorobiaceae ) | |
| Bacterioclorofila g | 408, 418, 470, 575, 763 (¿en qué?) 412, 788 ( in vivo ) | Heliobacterias |
biosíntesis
La clorofila se encuentra en eucariotas en los cloroplastos sintetizados en procariotas en el citoplasma . En el caso de muchos fotótrofos , la formación de clorofila es inducida por la luz y no ocurre sin exposición. La biosíntesis consta de una serie de numerosos pasos con un número correspondiente de enzimas específicas .
La síntesis de este y otros tetrapirroles es un proceso de varios pasos que también tiene varios puntos de ramificación. La biosíntesis comienza a partir de L - glutamato y termina en un sirohema -, un hemo - y una rama de clorofila.
Después de varios pasos, se forma el uroporfirinógeno III a partir de L- glutamato , el primer punto de ramificación a partir del cual se puede formar el sirohema. Luego, el uroporfirinógeno III se convierte en protoporfirina IX en tres pasos , que es el segundo punto de ramificación del hemo. En la protoporfirina IX, el ion magnesio se introduce en una reacción dependiente de ATP, que cataliza una quelatasa de magnesio ( EC 6.6.1.1 ). La protoporfirina IX de Mg formada de esta manera se convierte en protoclorofilida de vinilo a mediante el éster monoetílico de protoporfirina IX de Mg . Ese paso es catalizado por una ciclasa que introduce el quinto anillo en la clorofila. En las plantas, esta enzima es dependiente de O 2 , mientras que en los procariotas hay ciclasas tanto dependientes como independientes de O 2 .
En el siguiente paso, el anillo D de la protocloropila se reduce a divinil clorofilida a por una oxidorreductasa ( EC 1.3.1.33 ) . En las angiospermas, esta reacción es absolutamente dependiente de la luz. Por lo tanto, las plántulas no forman clorofila hasta que se exponen a la luz. Otras plantas (algunas gimnospermas ), algas, pero también cianobacterias tienen una oxidorreductasa tanto dependiente de la luz como independiente de la luz. Como resultado, estos organismos pueden sintetizar clorofila incluso en la oscuridad. Divinil chlorophylid a se reduce a monovinil chlorophylid una por una reductasa antes de que este se esterifica a la clorofila a en una etapa final utilizando fosfato de fitol . Este paso terminal está catalizado por una clorofila sintasa, una prenil transferasa ( EC 2.5.1.62 ).
La clorofila b también puede ser formada a partir de clorofila una o viceversa.
La descomposición de la clorofila en árboles de hoja caduca produce un color característico de las hojas en otoño. La clorofila es metabolizada a clorofilida por la clorofilasa . A esto le sigue un intercambio iónico de Mg 2+ - Dequelatasa a feofórbido . El feofórbido es oxidado por el feofórbido A oxigenasa con el cofactor ferredoxina , por lo que el color verde desaparece y primero surgen varios productos de degradación fluorescente (FCC, de catabolitos de clorofila fluorescente ingleses ) y en la degradación posterior sustancias no fluorescentes (NCC). En Maple Chlorophyll es otra vía desmantelada hacia Dioxobilan .
Importancia en la fotosíntesis
Las clorofilas tienen varias tareas dentro de la fotosíntesis en el fotosistema I y el fotosistema II . Con mucho, la mayor parte se utiliza para la absorción de luz y la transmisión de la energía absorbida. Entonces actúan como fotosensibilizadores . Para ello, las moléculas de clorofila se organizan en complejos captadores de luz , los cuales se disponen de tal manera que por un lado se forma la mayor superficie absorbente posible y por otro lado se crea un embudo energético que guía la energía absorbida hacia el llamado centro de reacción . En el centro de reacción, dos clorofilas sirven como aceptores de esta energía. Están dispuestos de manera tan especial que su excitación conduce a una separación de carga, que puede considerarse como el primer paso en la fotosíntesis real. Este par de clorofila se llama par especial en inglés .
Existen muchas diferencias en la estructura de los complejos captadores de luz en los muy diferentes organismos que impulsan la fotosíntesis, pero el centro de reacción casi siempre está estructurado de la misma manera. En plantas, algas y cianobacterias, el par especial siempre está formado por clorofila a , en bacterias por diversas bacterioclorofilas.
Aparición en los alimentos
El contenido de clorofila es particularmente alto en vegetales verdes. La clorofila a y b contenido de verduras y fruta por 100 g de sustancia fresco se enumeran en la tabla siguiente con el fin de clorofila descendente un contenido:
| Clorofila a | Clorofila b | |
|---|---|---|
| col rizada | 189 magnesio | 41 magnesio |
| Ortiga grande | 185 magnesio | 173 magnesio |
| perejil | 157 magnesio | 55 magnesio |
| Espinacas | 95 magnesio | 20 magnesio |
| Brócoli | 26 magnesio | 6 mg |
| judías verdes | 12 mg | 4 mg |
| guisantes verdes | 10 mg | 2 mg |
| pepino | 6 mg | 2 mg |
| Fruta de kiwi | 1,7 mg | 0,4 mg |
| repollo blanco | 0,3-1 mg | 0,1-0,2 mg |
Con la etiqueta E 140 , las clorofilas ( CI Natural Green 3 ) están aprobadas como colorante alimentario .
Cada vez más estudios muestran que las sustancias vegetales secundarias tienen un efecto positivo en los procesos metabólicos humanos. Esto se aplica tanto a la clorofila como a los flavonoides y carotenoides , por ejemplo .
historia
Las primeras descripciones de un " tinte " que puede extraerse con etanol ("alcohol de vino") y descomponerse bajo la influencia de la luz se pueden encontrar en el libro de Heinrich Friedrich Link "Enseñanzas básicas de anatomía y fisiología de las plantas", Gotinga 1807. Allí también son ambiguos. Evidencia de que Joseph Louis Proust describió el tinte verde como "Fécule". Pierre Joseph Pelletier y Joseph Bienaimé Caventou extrajeron la sustancia nuevamente y la llamaron clorofila . Los primeros estudios sobre la estructura química de la clorofila provienen de Richard Willstätter (1913). El químico Hans Fischer reanudó la investigación de Willstätter en la década de 1930 y en 1940 pudo dilucidar la estructura de la molécula. La investigación de Fischer fue confirmada en 1960 por la síntesis de clorofila de Robert B. Woodward . Incluso antes de Woodward, la síntesis total tuvo éxito de una manera algo diferente por un grupo de químicos en el antiguo lugar de trabajo de Fischer, la Universidad Técnica de Munich. Los ex empleados de Fischer, Alfred Treibs y Martin Strell, continuaron allí su trabajo sobre la síntesis total de clorofila. El objetivo de ambos grupos era la síntesis de feofórbido a , ya que Willstätter ya había descrito la síntesis residual en base a esta.
diverso
Una propiedad importante de la clorofila es la fluorescencia de la clorofila . Se utiliza principalmente para determinar el contenido de clorofila y su actividad, así como para otros análisis científicos.
Debido a su efecto neutralizador de olores, la clorofila también está disponible en forma de tabletas en las farmacias como remedio para el mal aliento y el olor corporal.
Ver también
literatura
- Hans W. Heldt y Birgit Piechulla: bioquímica vegetal . 4ª edición. Spectrum Academic Publishing House, 2008, ISBN 978-3-8274-1961-3 .
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Bioquímica . 6ª edición. Editorial Académica Spectrum, Heidelberg 2007, ISBN 978-3-8274-1800-5 .
- R. Tanaka, A. Tanaka: Biosíntesis de tetrapirrol en plantas superiores . En: Annu Rev Plant Biol . 58; 321-346; PMID 17227226 . 2007; doi: 10.1146 / annurev.arplant.57.032905.105448
enlaces web
- Vía metabólica para la formación de clorofila y hemo en enzimas KEGG
- Espectros de absorción de la Universidad de Salud y Ciencias de Oregon
Evidencia individual
- ^ Andreas Bresinsky, Christian Körner, Joachim W. Kadereit, G. Neuhaus y Uwe Sonnewald: Strasburger - Libro de texto de botánica . 36ª edición. Spektrum Akademischer Verlag, Heidelberg 2008, p. 315, ISBN 978-3-8274-1455-7 ; Pág. 277.
- ^ Ian Fleming : Configuración absoluta y la estructura de la clorofila , Nature 1967, 216 , 151-152 doi: 10.1038 / 216151a0 .
- ↑ Hyper Physics: colores espectrales
- ^ Hugo Scheer (editor): Clorofilas. CRC Press, 1991. ISBN 0-8493-6842-1 .
- ↑ a b c d Gerhard G. Habermehl , Peter E. Hammann, Hans C. Krebs, W. Ternes: Naturstoffchemie. Una introducción . 3. Edición. Springer, Berlín 2008, ISBN 978-3-540-73732-2 , págs. 530 .
- ↑ a b c d e f g h Michael T. Madigan, John M. Martinko: Brock - microbiología . 11ª edición. Pearson Studium, Munich / Boston et al.2009, ISBN 978-3-8273-7358-8 , pág. 607 (Inglés: Biología de microorganismos de Brock . Traducido por Thomas Lazar, Freya Thomm-Reitz).
- ↑ Samuel I. Beale: Enzimas de la biosíntesis de clorofila (artículo de revisión). En: Investigación de la fotosíntesis . Vol. 60, 1999. págs. 43-73. La ruta de la biosíntesis también se muestra aquí.
- ↑ Hans W. Heldt y Birgit Piechulla: Bioquímica vegetal. 4ª edición. Spektrum Akademischer Verlag, 2008, ISBN 978-3-8274-1961-3 , pág.292.
- ^ A b T. Müller, M. Rafelsberger, C. Vergeiner, B. Kräutler: Un dioxobilano como producto de una ruta divergente de descomposición de la clorofila en el arce de Noruega. En: Angewandte Chemie. Volumen 50, número 45, noviembre de 2011, págs.10724-10727, doi : 10.1002 / anie.201103934 , PMID 21928453 , PMC 3262146 (texto completo libre).
- ↑ a b c P. Matile, S. Hortensteiner, H. Thomas, B. Krautler: Desglose de clorofila en hojas senescentes. En: Fisiología vegetal. Volumen 112, Número 4, diciembre de 1996, págs.1403-1409 , PMID 12226455 , PMC 158071 (texto completo libre).
- ↑ Entrada sobre E 140: Clorofilas y clorofilinas en la base de datos europea de aditivos alimentarios, consultada el 16 de junio de 2020.
- ↑ Especificaciones de los aditivos alimentarios permitidos
- ↑ Fitoquímicos y sus efectos en la salud: una actualización basada en el Informe de nutrición de 2012. Consultado el 15 de abril de 2021 .
- ↑ Pelletier & Caventou, Sur la Matiere verte des Feuilles Annales de Chimie et de Physique , 1818, 9, 194-196 ( vista previa limitada en la búsqueda de libros de Google).
- ↑ M. Strell, A. Kalojanoff, H. Koller, síntesis parcial de la estructura básica de la clorofila a, de feofórbido a , Angew. Chem. 72, 169-170 (1960).
- ↑ Eric Fontain, La síntesis de clorofila de Munich , TU Munich, 2000