Frederick Sanger
Frederick Sanger OM , CH , CBE (nacido el 13 de agosto de 1918 en Rendcomb , Gloucestershire , † el 19 de noviembre de 2013 en Cambridge , Cambridgeshire ) fue un bioquímico británico .
Fue una de las pocas personas que fue galardonada dos veces con el Premio Nobel: en 1958, Sanger recibió el Premio Nobel de Química (como único ganador) por el esclarecimiento de la estructura de la insulina y su trabajo sobre la secuenciación de proteínas . En 1980 fue nuevamente galardonado con el Premio Nobel de Química (junto con Paul Berg , nacido en 1926, y Walter Gilbert , nacido en 1932), esta vez por sus investigaciones sobre la determinación de la secuencia de bases en ácidos nucleicos .
Vida
Escuela y estudio
Frederick Sanger nació como el segundo hijo del doctor Dr. Frederick Sanger senior (1876-1937) y Cicely Sanger (1880-1938) nacieron en Rendscomb. Influenciado por su padre y su hermano mayor de un año, Theodore, Sanger desarrolló un interés en las ciencias naturales a una edad temprana . Tras finalizar sus estudios en Bryanston School y, a partir de 1936, en St John's College en Cambridge , en un principio quiso estudiar medicina, pero luego se decidió por la bioquímica , ya que como científico, a diferencia de la profesión médica, podía concentrarse más en un tema y así quizás lograr más. Entonces Sanger comenzó a estudiar bioquímica en el Departamento de Bioquímica de Cambridge.
En 1939, Sanger recibió su licenciatura en artes . Desde que llegó desde un Quaker familia, se negó el servicio militar por razones de conciencia y continuó trabajando en su tesis doctoral durante la Segunda Guerra Mundial , lo que estaba haciendo en el mismo instituto bajo la supervisión de A. Neuberger en el metabolismo de la lisina de aminoácidos . En 1943 recibió su doctorado .
Actividad investigadora
El trabajo de Sanger fue apoyado por una subvención de Beit Memorial Fellowship for Medical Research de 1944 a 1951 . En 1951 se convirtió en empleado externo del Medical Research Council (MRC).
En el año de su doctorado , Albert Chibnall sucedió a Frederick Gowland Hopkins como director de bioquímica en Cambridge, y Sanger se convirtió en miembro del grupo de investigación de Chibnall. El principal interés del grupo fue la química de las proteínas, especialmente la de la insulina . En 1945, Sanger finalmente desarrolló un método para determinar la secuencia de aminoácidos , con la ayuda del cual determinó completamente la secuencia de insulina durante un período de doce años. En 1955 se publicó la secuencia de 51 aminoácidos dispuestos en una cadena en la insulina, por lo que Sanger recibió el Premio Nobel de Química en 1958 .
Como resultado, Sanger se quedó en Cambridge y en 1962 se convirtió en jefe del departamento de química de proteínas en el Laboratorio de Biología Molecular (LMB). Este instituto fue construido en 1962 como un nuevo complejo de laboratorio después de que el Medical Research Council creara un grupo en Cambridge en 1947 para "estudiar la estructura molecular de los sistemas biológicos". Aunque Sanger no había estado particularmente interesado en los ácidos nucleicos hasta entonces , a través de discusiones con científicos como Francis Crick y Sydney Brenner, reconoció la necesidad de determinar también la secuencia de este otro biopolímero . Por lo tanto, en los años siguientes, Sanger se dedicó al desarrollo de otro método de secuenciación, que finalmente condujo al "método de terminación de cadena " en 1975 . En 1977, se presentó al mundo por primera vez la secuenciación de ADN basada en el genoma completamente descifrado de un bacteriófago. En 1980, Sanger recibió el Premio Nobel de Química por segunda vez por sus contribuciones a la secuenciación de ácidos nucleicos.
En 1983 se jubiló Frederick Sanger. Más recientemente se dedicó a sus aficiones junto con su esposa Margaret Joan: la jardinería y la navegación. Tienen tres hijos de su matrimonio. Frederick Sanger murió el 19 de noviembre de 2013 en Cambridge.
Premios
- 1951 Medalla Corday Morgan de la Royal Society of Chemistry
- 1954 Nombramiento como miembro de la Royal Society (FRS)
- 1958 miembro de la Academia Estadounidense de Artes y Ciencias
- 1958 y 1980: Premio Nobel de Química. En la historia del Premio Nobel, solo cuatro científicos han logrado recibir este máximo honor dos veces (además de Sanger, estos fueron Marie Curie , Linus Pauling y John Bardeen . Sanger y Bardeen son también las únicas personas que han sido galardonadas con el Premio Nobel dos veces en se convirtió en la misma disciplina).
- 1963 Galardonado con el Comandante de la Orden del Imperio Británico (CBE) por la reina Isabel II.
- 1967 miembro de la Academia Nacional de Ciencias
- En 1969 Sanger recibió la Medalla Real de la Royal Society .
- 1971, Premio Internacional de la Fundación Gairdner de 1979
- 1977 Medalla Copley de la Royal Society
- 1979 Premio Albert Lasker de Investigación Médica Básica
- 1981 Admisión a la Orden de los Compañeros de Honor (CH)
- En 1986 Sanger fue aceptado en la Orden del Mérito (OM) por Isabel II , cuya membresía regular está limitada a solo 24 personas.
- En 1988 Sanger se convirtió en miembro correspondiente de la Academia de Ciencias de Baviera .
- El Centro Sanger , que lleva el nombre de Frederick Sanger, fue fundado en Cambridge en 1992 con el objetivo de secuenciar e investigar el genoma humano y los genomas de otros organismos.
- En 1997, se amplió el Departamento de Bioquímica de la Universidad de Cambridge, donde Sanger había trabajado hasta 1962. Además del "Edificio Hopkins", ahora hay un segundo, el "Edificio Sanger".
planta
Método para determinar la secuencia de aminoácidos.
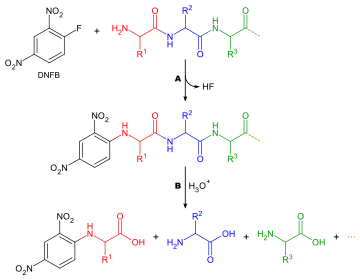
El método de Sanger para determinar la secuencia de aminoácidos se originó durante su tiempo como miembro del grupo de investigación de Albert Chibnall en Cambridge. En la década de 1940, la química de las proteínas experimentó una revolución con el desarrollo de métodos eficientes de separación cromatográfica de proteínas , péptidos y aminoácidos . Sanger ahora quería determinar el orden de los aminoácidos en una proteína ( secuencia de aminoácidos ). Para hacer esto, primero desmanteló la cadena de proteínas en pequeños fragmentos de péptidos y luego los aisló utilizando los nuevos métodos. Para marcar y luego identificar el aminoácido terminal, Sanger convirtió el fragmento de péptidos con 1-fluoro-2,4-dinitrobenceno . Los péptidos derivatizados en el extremo N se escindieron completamente en sus aminoácidos, cuyas cantidades relativas se determinaron luego cuantitativamente. La identidad del aminoácido terminal se pudo determinar mediante análisis cromatográfico del derivado de dinitrofenilo (DNP) coloreado. En esta operación se obtuvieron dos datos: 1. la identidad del primer aminoácido de la cadena y 2. la naturaleza de los otros aminoácidos de la cadena (aunque no su posición). Repitiendo el procedimiento varias veces, finalmente se pueden sacar conclusiones sobre la secuencia original. La figura ilustra el principio del método de secuenciación en un péptido pequeño.
En doce años de trabajo, Sanger logró determinar la secuencia completa de insulina. Para empeorar las cosas, la insulina es una proteína que consta de dos cadenas polipeptídicas unidas por puentes disulfuro . También hubo que determinar la disposición de estos puentes. En 1955 se publicó la secuencia completa de insulina. Esto demostró por primera vez que las proteínas tienen una estructura química única. Las hipótesis anteriores ahora podrían finalmente rechazarse, como la de que las proteínas tienen una composición de aminoácidos definida, pero con una secuencia aleatoria, o que las proteínas son incluso agregados de unidades similares más pequeñas. En 1958 Sanger recibió el Premio Nobel de Química por este trabajo .
El método de secuenciación de Sanger fue posteriormente reemplazado por la degradación de isotiocianato de fenilo desarrollada por el bioquímico sueco Pehr Edman . La principal ventaja del método de Edman era que los aminoácidos podían descomponerse e identificarse sucesivamente desde el extremo N. El péptido restante, acortado en un aminoácido, podría luego someterse a otro ciclo de degradación y la secuencia podría determinarse con relativa rapidez.
Método para secuenciar ácidos nucleicos
El método de Sanger para secuenciar ácidos nucleicos se originó durante su tiempo como jefe del departamento de química de proteínas en el Laboratorio de Biología Molecular (LMB) en Cambridge. Surgió de la necesidad de determinar la secuencia de las nucleobases .
Para lograr este objetivo, Sanger desarrolló primero un método de secuenciación de ácidos ribonucleicos (ARN), que luego aplicó al ácido desoxirribonucleico (ADN). Sin embargo, este método fue muy lento y solo permitió la determinación de secciones de secuencia corta. En los años siguientes, desarrolló un nuevo método que se convertiría en la base del método actual de secuenciación del ADN , el llamado método didesoxi. Esta técnica utiliza las siguientes propiedades del ADN:
- El ADN es una molécula de doble hebra , similar a una escalera de cuerda sinuosa. Los peldaños de la escalera forman pares de nucleobases ( adenina , guanina , timina y citosina ), de las cuales solo hay dos combinaciones: la adenina es opuesta a la timina, la citosina está emparejada con la guanina.
- Si las dos hebras simples están separadas, la hebra complementaria se puede sintetizar con la ayuda de una ADN polimerasa . Sin embargo, necesita una pequeña pieza complementaria de ADN ( cebador ) que esté unida a la hebra única y extendida por la polimerasa de acuerdo con las instrucciones de la hebra opuesta (hebra plantilla).
La pieza de ADN sintetizada tiene así un punto de partida definido. Sin embargo, los productos de síntesis pueden tener diferentes longitudes; la longitud depende de cuántos nucleótidos libres estén disponibles para la síntesis o de si la polimerasa se cae accidentalmente de la hebra molde.

dNTP es la abreviatura general de un trifosfato de nucleósido y puede significar dATP, dCTP, dGTP o dTTP. Los ddNTP son las variantes didesoxi correspondientes de los dNTP. La incorporación de un ddNTP conduce a la terminación de la reacción de polimerización. Los puntos azules en el extremo 5 'del cebador representan una marca (por ejemplo, un grupo fluorescente) por medio de la cual los productos de síntesis pueden hacerse visibles más tarde en el gel. Alternativamente, también se pueden usar nucleósidos trifosfatos marcados radiactivamente para la reacción de polimerización.
El truco de Sanger ahora es llevar a cabo la reacción de polimerización en cuatro enfoques separados, y asegurarse de que cada hebra tenga el mismo comienzo (que viene dado por el cebador) y que la reacción de extensión, aunque en puntos diferentes, siempre ocurra en un tipo determinado. de base debe terminar. Para garantizar esto, cada mezcla de reacción contiene los cuatro monómeros de nucleótidos , así como la variante didesoxi de un tipo de nucleótido. La extensión de la cadena continúa hasta que finalmente se incorpora un didesoxi nucleótido en algún momento. Esto significa que falta el grupo 3'-OH para la formación del enlace fosfodiéster con el siguiente eslabón de la cadena y la síntesis se detiene aquí. Al definir el punto de partida, la longitud de los fragmentos de síntesis en una mezcla de reacción refleja la posición relativa del tipo de base nucleica respectiva en la molécula. Si se utilizan nucleótidos radiactivos (o marcados de otro modo) para la reacción y se separan los cuatro enfoques uno al lado del otro según su tamaño en un gel de acrilamida , la secuencia de bases se puede leer directamente del gel. La figura de la derecha ilustra el principio de secuenciación didesoxi.
En 1977 Sanger y colaboradores presentaron la secuencia completa del bacteriófago φX174 de 5.386 pares de bases . La secuencia de aminoácidos de las diez proteínas virales podría leerse directamente de la secuencia de este virus bacteriano, ya que el código genético , que indica qué secuencia de tres nucleobases ( triplete de bases ) codifica para qué aminoácido en una proteína, se conocía a través de los pioneros trabajar en la década de 1960. En 1980, Sanger recibió el Premio Nobel por segunda vez por sus contribuciones a la secuenciación de ácidos nucleicos.
La importancia del trabajo de Sanger para la ingeniería genética y el proyecto del genoma
A principios de la década de 1970, se desarrollaron métodos de clonación con los que se pueden reproducir en bacterias fragmentos de ADN de cualquier origen para que haya suficiente material disponible para la secuenciación. Esto abrió la posibilidad de secuenciar toda la información genética de un organismo, el genoma , y así derivar indirectamente las secuencias de todas las proteínas que teóricamente pueden ser sintetizadas por este organismo. Junto con Stanley Norman Cohen y Paul Berg , los inventores de la técnica de clonación recombinante, Frederick Sanger puede describirse como el padre de la ingeniería genética y el proyecto del genoma.
Citas
“De las tres actividades principales involucradas en la investigación científica, pensar, hablar y hacer, prefiero la última y probablemente la mejor. Estoy bien pensando, pero no muy bien hablando ".
“Anteriormente no había tenido mucho interés en los ácidos nucleicos. Solía ir a las conferencias Gordon sobre proteínas y ácidos nucleicos cuando los dos sujetos estaban entre corchetes, y me sentaba a escuchar las charlas sobre ácidos nucleicos esperando volver a las proteínas. Sin embargo, con gente como Francis Crick alrededor, era difícil ignorar los ácidos nucleicos o no darse cuenta de la importancia de secuenciarlos ".
“A diferencia de muchos científicos, decidí retirarme y dejar la investigación cuando cumplí 65 años. Esto sorprendió a mis colegas y, en cierta medida, también a mí mismo. No había pensado en la jubilación hasta que de repente me di cuenta de que en unos pocos años tendría 65 años y tendría derecho a dejar de trabajar y hacer algunas de las cosas que siempre había querido hacer y para las que nunca había tenido tiempo. La posibilidad parecía sorprendentemente atractiva, sobre todo porque nuestro trabajo había alcanzado un clímax con el método de secuenciación del ADN y, más bien, sentí que continuar sería una especie de anticlímax ".
suerte
Obras originales importantes:
- Para secuenciación de proteínas
- F. Sanger: Los grupos amino libres de insulina. En: Biochemical Journal . Volumen 39, núm. 5, 1945, págs. 507-515; PMID 16747948 ; PMC 1258275 (texto completo gratuito).
- F. Sanger: Los péptidos terminales de la insulina. En: Biochemical Journal. Volumen 45, 1949, págs. 563-574; PMID 15396627 ; PMC 1275055 (texto completo gratuito).
- AP Ryle, F. Sanger, R. Kitai: Los enlaces disulfuro de la insulina. En: Biochemical Journal. Volumen 60, 1955, págs. 541-556; PMID 13249947 ; PMC 1216151 (texto completo gratuito).
- Para secuenciación de ADN
- F. Sanger, S. Nicklen, AR Coulson: secuenciación de ADN con inhibidores de terminación de cadena. En: Actas de la Academia Nacional de Ciencias . Volumen 74, 1977, págs. 5463-5467; PMID 271968 ; PMC 431765 (texto completo gratuito).
- F. Sanger, GM Air, BG Barrell, NL Brown, AR Coulson, CA Fiddes, CA Hutchison, PM Slocombe, M. Smith: Secuencia de nucleótidos del ADN del bacteriófago phi X174. En: Naturaleza . Volumen 265, 1977, págs. 687-695; PMID 870828 .
- Autobiográfico, artículo de revisión
- F. Sanger: Secuencias, secuencias y secuencias. En: Revisión anual de bioquímica . Volumen 57, 1988, págs. 1-28; PMID 2460023 .
- F. Sanger: Los primeros días de las secuencias de ADN. En: Nature Medicine . Volumen 7, 2001, págs. 267-268.
literatura
- John Walker: Frederick Sanger (1918-2013). En: Naturaleza . Volumen 505, 2014, p. 27, doi: 10.1038 / 505027a
- Sydney Brenner: Frederick Sanger (1918-2013). En: Ciencia . Volumen 343, No. 6168, 2013, p. 262, doi: 10.1126 / science.1249912
enlaces web
- Información de la Fundación Nobel sobre la ceremonia de entrega de premios de 1958 para Frederick Sanger
- Información de la Fundación Nobel sobre la concesión del premio de 1980 a Frederick Sanger
- Wellcome Trust Sanger Institute
- Autobiografía
Evidencia individual
- ↑ a b Alok Jha: el pionero del ADN Frederick Sanger muere a los 95 años ( inglés ) En: The Guardian . 20 de noviembre de 2013. Archivado desde el original el 21 de noviembre de 2013. Recuperado el 21 de noviembre de 2013.
- ^ Academia de Ciencias de Baviera: miembros correspondientes . En: badw.de . Academia de Ciencias de Baviera. Archivado desde el original el 7 de noviembre de 2011. Consultado el 21 de noviembre de 2013.
- ↑ Frederick Sanger: Secuencias, secuencias y secuencias . En: Frederick Sanger, Margaret Dowding (Eds.): Documentos seleccionados de Frederick Sanger: con comentarios . World Scientific, Singapur / River Edge / Londres 1996, ISBN 981-02-2430-3 , págs. 635 (Introducción).
- ↑ Frederick Sanger: Secuencias, secuencias y secuencias . En: Frederick Sanger, Margaret Dowding (Eds.): Documentos seleccionados de Frederick Sanger: con comentarios . World Scientific, Singapur / River Edge / Londres 1996, ISBN 981-02-2430-3 , págs. 648 .
- ↑ Frederick Sanger: Secuencias, secuencias y secuencias . En: Frederick Sanger, Margaret Dowding (Eds.): Documentos seleccionados de Frederick Sanger: con comentarios . World Scientific, Singapur / River Edge / Londres 1996, ISBN 981-02-2430-3 , págs. 660 .
| información personal | |
|---|---|
| APELLIDO | Sanger, Frederick |
| BREVE DESCRIPCIÓN | Bioquímico británico y premio Nobel de química |
| FECHA DE NACIMIENTO | 13 de agosto de 1918 |
| LUGAR DE NACIMIENTO | Rendcomb , Reino Unido |
| FECHA DE MUERTE | 19 de noviembre de 2013 |
| LUGAR DE LA MUERTE | Cambridge , Reino Unido |